El Departamento de Bioquímica y Biología Molecular de la UCM en colaboración con un grupo del Barcelona Supercomuter Center (liderado por Víctor Guallar) y del Instituto de Catálisis y Petroleoquímica del CSIC (liderado por Manuel Ferrer),han publicado un artículo en Nature Catalysis describiendo un nuevo método para la degradación de nanoplásticos, con mayor eficacia que otros conocidos, y a temperatura ambiente.
El proyecto se ha basado en la transformación de una proteína del veneno de una anémona marina, común en nuestros mares, para convertirla en un nanorreactor capaz de degradar partículas.
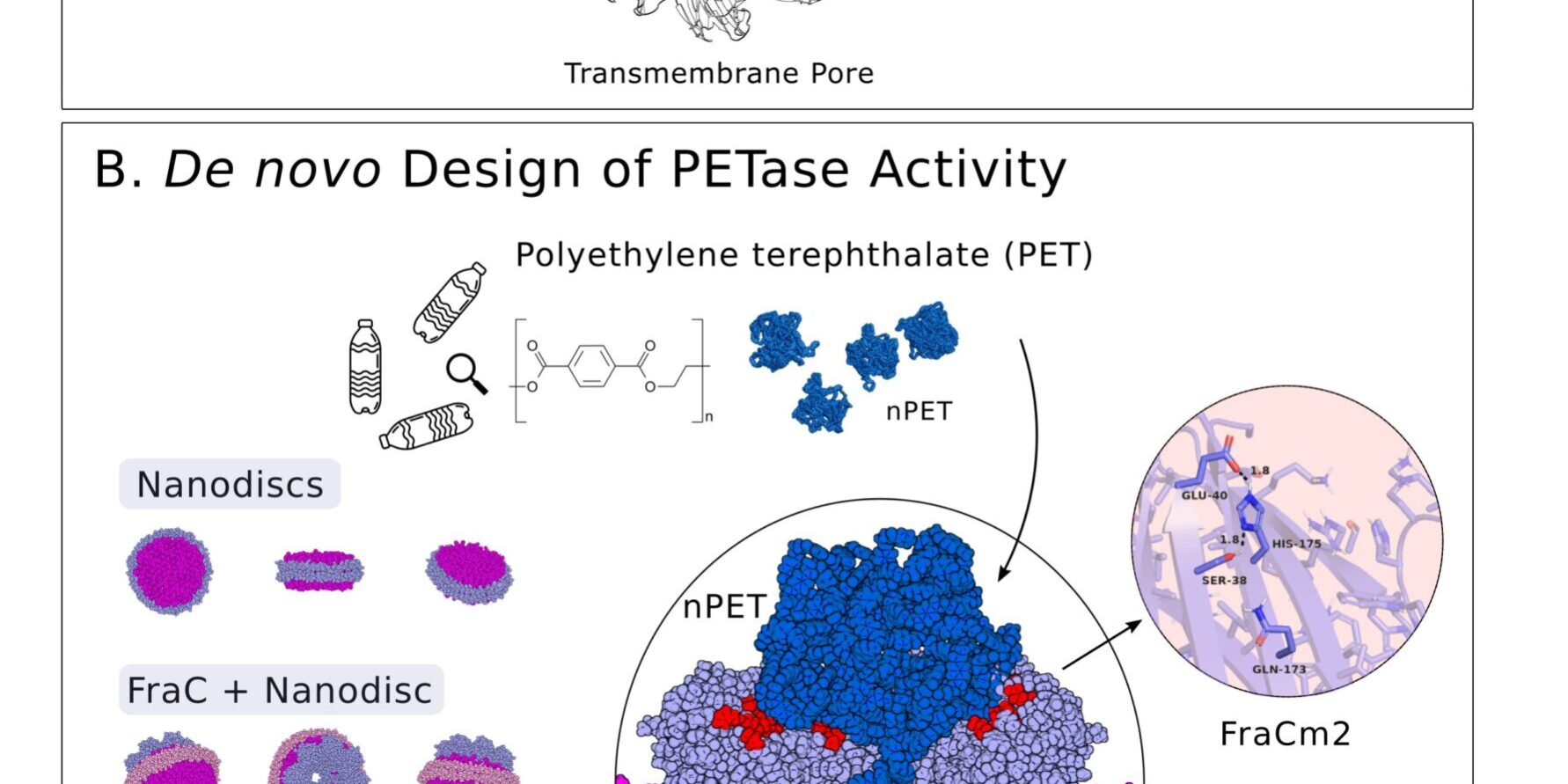
El tereftalato de polietileno (PET) es un plástico común que se encuentra no solo en botellas y envases (los típicos de plástico transparente), sino también en forma de micropartículas que llegan a los ecosistemas. En este trabajo han diseñado nanoporos artificiales proteicos que pueden descomponer los microplásticos de PET.
Para lograr esto, usaron una proteína del veneno de la anémona fresa (Actinia fragacea) y emplearon métodos computacionales para añadir sitios reactivos artificiales, con una geometría (algo muy importante en un catalizador) que se asemeja mucho a la de la enzima PETasa que se encuentra en la bacteria Ideonella sakaiensis y que es una de las más eficaces a la hora de degradar PET, pero que funciona eficazmente solo a 70ºC. Cuando se ensamblaron estas proteínas artificiales en nanoporos, fueron capaces de descomponer los microplásticos de PET, de un tamaño que va desde submicro (menos de una millonésima de metro) hasta el nano (milmillonésima parte de un metro; el grosor de un billete de banco son cien mil nanometros), y a temperatura ambiente.
Consultar el artículo completo aquí.